化学原理、化学实验是高中化学考试中常出现的考点,北京高考资讯最新整理的高中化学三年的《化学反应原理》,记得收藏学习!
第一章 化学反应与能量
考点1:吸热反应与放热反应
②活泼金属与酸或水的反应;
③酸碱中和反应;
④铝热反应;
⑤大多数化合反应(但有些化合反应是吸热反应,如:N2+O2=2NO,CO2+C=2CO等均为吸热反应)。
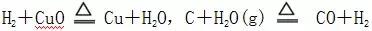 等也是吸热反应;
等也是吸热反应;考点2:反应热计算的依据
1、根据热化学方程式计算
反应热与反应物各物质的物质的量成正比。
2、根据反应物和生成物的总能量计算
ΔH=E生成物-E反应物。
3、根据键能计算
ΔH=反应物的键能总和-生成物的键能总和。
4、根据盖斯定律计算
化学反应的反应热只与反应的始态(各反应物)和终态(各生成物)有关,而与反应的途径无关。即如果一个反应可以分步进行,则各分步反应的反应热之和与该反应一步完成时的反应热是相同的。
温馨提示:
①盖斯定律的主要用途是用已知反应的反应热来推知相关反应的反应热。
②热化学方程式之间的“+”“-”等数学运算,对应ΔH也进行“+”“-”等数学计算。
5、根据物质燃烧放热数值计算:Q(放)=n(可燃物)×|ΔH|。
第二章 化学反应速率与化学平衡
考点1:化学反应速率
1、化学反应速率的表示方法___________。
化学反应速率通常用单位时间内反应物浓度和生成物浓度的变化来表示。表达式:___________ 。
其常用的单位是__________ 或__________ 。
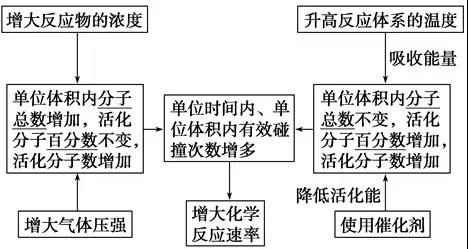
2、影响化学反应速率的因素
(1)内因(主要因素):反应物本身的性质。
(2)外因(其他条件不变,只改变一个条件)

3、理论解释——有效碰撞理论
(1)活化分子、活化能、有效碰撞
①活化分子:能够发生有效碰撞的分子。
②活化能:如图
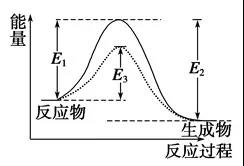
图中:E1为正反应的活化能,使用催化剂时的活化能为E3,反应热为E1-E2。(注:E2为逆反应的活化能)
③有效碰撞:活化分子之间能够引发化学反应的碰撞。
考点2:化学平衡
1、化学平衡状态:一定条件(恒温、恒容或恒压)下的可逆反应里,正反应和逆反应的速率相等,反应混合物(包括反应物和生成物)中各组分的浓度保持不变的状态。

3、判断化学平衡状态的依据
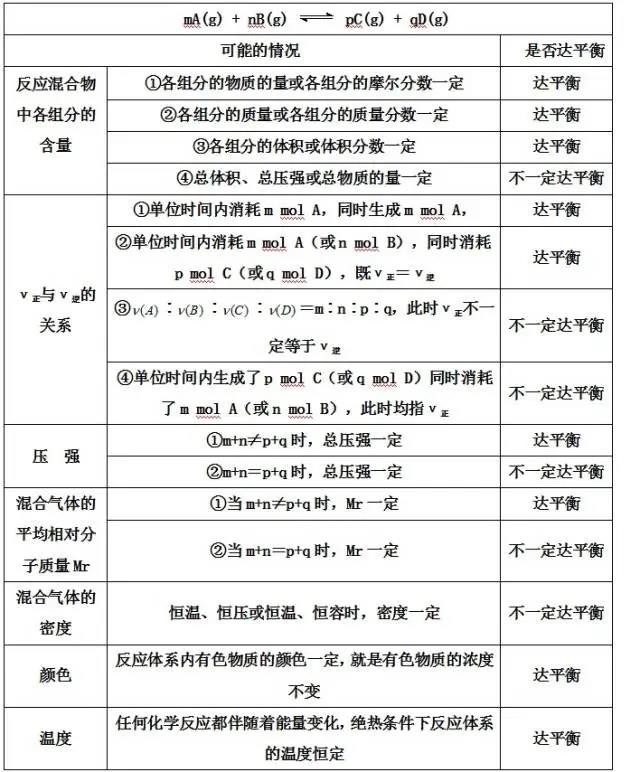
考点3:化学平衡的移动
1、概念
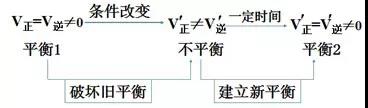
可逆反应中旧化学平衡的破坏、新化学平衡的建立,由原平衡状态向新化学平衡状态的转化过程,称为化学平衡的移动。
2、化学平衡移动与化学反应速率的关系
(1)v正>v逆:平衡向正反应方向移动。
(2)v正=v逆:反应达到平衡状态,不发生平衡移动。
(3)v正<v逆:平衡向逆反应方向移动。
3、“惰性气体”对化学平衡的影响
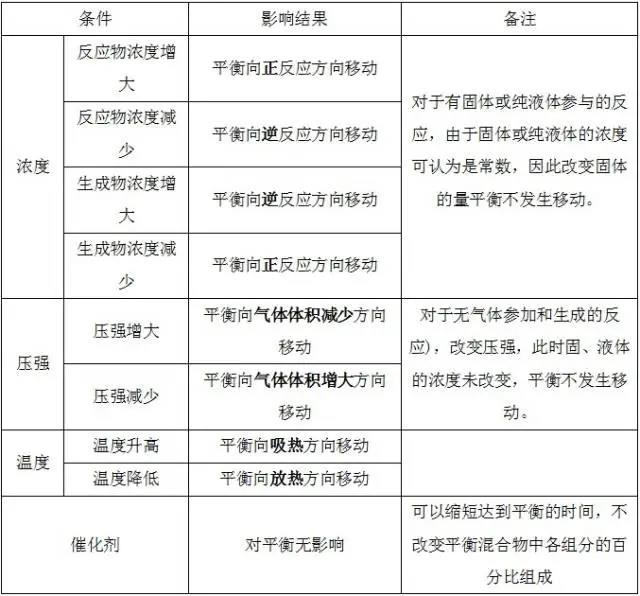
①恒温、恒容条件
 体系总压强增大→体系中各组分的浓度不变→平衡不移动。
体系总压强增大→体系中各组分的浓度不变→平衡不移动。原平衡体系 容器容积增大,各反应气体的分压减小→体系中各组分的浓度同倍数减小
容器容积增大,各反应气体的分压减小→体系中各组分的浓度同倍数减小

4、勒夏特列原理
(1)定义:如果改变影响平衡的一个条件(如C、P或T等),平衡就向能够减弱这种改变的方向移动。
(2)原理适用的范围:已达平衡的体系、所有的平衡状态(如溶解平衡、化学平衡、电离平衡、水解平衡等)和只限于改变影响平衡的一个条件。
(3)勒夏特列原理中“减弱这种改变”的解释:外界条件改变使平衡发生移动的结果,是减弱对这种条件的改变,而不是抵消这种改变,也就是说:外界因素对平衡体系的影响占主要方面。
考点4:化学平衡常数
1、在一定温度下,当一个可逆反应达到平衡状态时,生成物的平衡浓度用化学方程式中的化学计量数作为指数的乘积与反应物的平衡浓度用化学方程式中的化学计量数作为指数的乘积的比值是一个常数,这个常数叫做化学平衡常数,简称平衡常数;用符号K表示。
2、平衡常数K的表达式:
对于一般的可逆反应:

,当在一定温度下达到化学平衡时,该反应的平衡常数为:
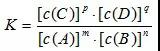
注意事项:
a、在平衡常数表达式中,反应物A、B和生成物C、D的状态全是气态,c(A)、c(B)、c(C)、c(D)均为平衡时的浓度。
b、当反应混合物中有固体或纯液体时,他们的浓度看做是一个常数,不写入平衡常数的表达式中。
c、平衡常数K的表达式与化学方程式的书写方式有关。
3、平衡常数K值的特征:
K值的大小与浓度、压强和是否使用催化剂无关。即对于一个给定的反应,在一定温度下,不论起始浓度(或压强)和平衡浓度(或压强)如何,也不论是否使用催化剂,达平衡时,平衡常数均相同。
4、平衡表达式K值的意义
K值表示可逆反应进行的程度:K值越大,正反应进行的程度越大(平衡时生成物的浓度大,反应物的浓度小),反应物的转化率越高;K值越小,正反应进行的程度越小,逆反应进行的程度越大,反应物的转化率越低。
考点5:反应物平衡转化率的计算公式

考点6:等效平衡
在一定条件(恒温恒容或恒温恒压)下,同一可逆反应体系,不管是从正反应开始,还是从逆反应开始,在达到化学平衡状态时,任何相同组分的百分含量(体积分数、物质的量分数等)均相同,这样的化学平衡互称等效平衡(包括“相同的平衡状态”)。
Ⅰ:恒温恒容条件下
①恒温恒容时,对一般的可逆反应,不同的投料方式如果根据化学方程式中计量系数比换算到同一边时,反应物(或生成物)中同一组分的物质的量完全相同,则互为等效平衡。此时一般不考虑反应本身的特点,计算的关键是换算到同一边后各组分要完全相同。
②恒温恒容时,对于反应前后气体分子数不变的可逆反应,不同的投料方式如果根据化学方程式中计量系数比换算到同一边时,只要反应物(或生成物)中各组分的物质的量的成比例,即互为等效平衡。此时的反应特点是无体积变化,计算的关键是换算到同一边后各组分只需要物质的量之比相同即可。
Ⅱ:恒温恒压条件下
在恒温恒压时,可逆反应以不同的投料方式进行反应,如果根据化学方程式中计量系数比换算,到同一边时,只要反应物(或生成物)中各组分的物质的量的成比例,即互为等效平衡。
第三章 水溶液中的离子平衡
考点1:弱电解质的电离

3、电离平衡:在一定的条件下,当电解质分子电离成 离子的速率 和离子结合成 时,电离过程就达到了 平衡状态 ,这叫电离平衡。
5、电离方程式的书写:用可逆符号 弱酸的电离要分布写(第一步为主)
考点2:水的电离和溶液的酸碱性
1、水电离平衡:
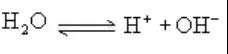
考点3:混合液的pH值计算方法
1、强酸与强酸的混合:(先求[H+]混:将两种酸中的H+离子物质的量相加除以总体积,再求其它) [H+]混=([H+]1V1+[H+]2V2)/(V1+V2)
2、强碱与强碱的混合:(先求[OH-]混:将两种酸中的OH‑离子物质的量相加除以总体积,再求其它) [OH-]混=([OH-]1V1+[OH-]2V2)/(V1+V2) (注意:不能直接计算[H+]混)
3、强酸与强碱的混合:(先据H++ OH-==H2O计算余下的H+或OH-,①H+有余,则用余下的H+数除以溶液总体积求[H+]混;OH-有余,则用余下的OH-数除以溶液总体积求[OH-]混,再求其它)
考点4:稀释过程溶液pH值的变化规律
考点5:强酸(pH1)强碱(pH2)混和计算规律
考点6:酸碱中和滴定
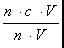
上述公式在求算浓度时很方便,而在分析误差时起主要作用的是分子上的V酸的变化,因为在滴定过程中c酸为标准酸,其数值在理论上是不变的,若稀释了虽实际值变小,但体现的却是V酸的增大,导致c酸偏高;V碱同样也是一个定值,它是用标准的量器量好后注入锥形瓶中的,当在实际操作中碱液外溅,其实际值减小,但引起变化的却是标准酸用量的减少,即V酸减小,则c碱降低了;对于观察中出现的误差亦同样如此。
综上所述,当用标准酸来测定碱的浓度时,c碱的误差与V酸的变化成正比,即当V酸的实测值大于理论值时,c碱偏高,反之偏低。
同理,用标准碱来滴定未知浓度的酸时亦然。
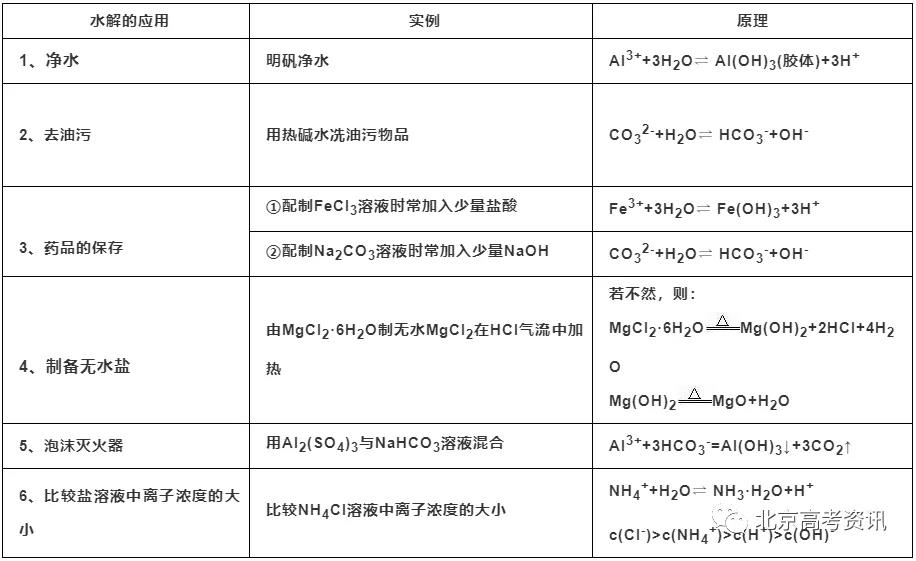
考点7:盐类的水解(只有可溶于水的盐才水解)
1、盐类水解:在水溶液中盐电离出来的离子跟水电离出来的H+或OH-结合生成弱电解质的反应。
2、水解的实质:水溶液中盐电离出来的离子跟水电离出来的H+或OH-结合,破坏水的电离,是平衡向右移动,促进水的电离。
3、盐类水解规律:
①有弱才水解,无弱不水解,越弱越水解;谁强显谁性,两弱都水解,同强显中性。
②多元弱酸根,浓度相同时正酸根比酸式酸根水解程度大,碱性更强。(如:Na2CO3>NaHCO3)
4、盐类水解的特点:
(1)可逆(与中和反应互逆)(2)程度小(3)吸热
5、影响盐类水解的外界因素:
①温度:温度越高,水解程度越大(水解吸热,越热越水解)
②浓度:浓度越小,水解程度越大 (越稀越水解)
③酸碱:促进或抑制盐的水解(H+促进阴离子水解而抑制阳离子水解;OH-促进阳离子水解而抑制阴离子水解)
6、酸式盐溶液的酸碱性:
①只电离不水解:如HSO4- 显 酸 性
②电离程度>水解程度,显酸性 (如: HSO3-、H2PO4-)
③水解程度>电离程度,显碱性(如:HCO3-、HS-、HPO42-)
7、双水解反应:
(1)构成盐的阴阳离子均能发生水解的反应。双水解反应相互促进,水解程度较大,有的甚至水解完全。使得平衡向右移。
(2)常见的双水解反应完全的为:Fe3+、Al3+与AlO2-、CO32-(HCO3-)、S2-(HS-)、SO32-(HSO3-);S2-与NH4+;CO32-(HCO3-)与NH4+其特点是相互水解成沉淀或气体。双水解完全的离子方程式配平依据是两边电荷平衡,如:2Al3++ 3S2- + 6H2O == 2Al(OH)3↓+3H2S↑
9、水解平衡常数(Kh)
对于强碱弱酸盐:Kh=Kw/Ka (Kw为该温度下水的离子积,Ka为该条件下该弱酸根形成的弱酸的电离平衡常数)
对于强酸弱碱盐:Kh=Kw/Kb(Kw为该温度下水的离子积,Kb为该条件下该弱碱根形成的弱碱的电离平衡常数)
电离、水解方程式的书写原则
1)多元弱酸(多元弱酸盐)的电离(水解)的书写原则:分步书写
注意:不管是水解还是电离,都决定于第一步,第二步一般相当微弱。
2)多元弱碱(多元弱碱盐)的电离(水解)书写原则:一步书写
考点8:溶液中微粒浓度的大小比较
☆☆基本原则:抓住溶液中微粒浓度必须满足的三种守恒关系:
①电荷守恒::任何溶液均显电中性,各阳离子浓度与其所带电荷数的乘积之和=各阴离子浓度与其所带电荷数的乘积之和
②物料守恒:(即原子个数守恒或质量守恒)
某原子的总量(或总浓度)=其以各种形式存在的所有微粒的量(或浓度)之和
③质子守恒:即水电离出的H+浓度与OH-浓度相等。
考点9:难溶电解质的溶解平衡
1、难溶电解质的溶解平衡的一些常见知识
(1)溶解度 小于 0.01g的电解质称难溶电解质。
(2)反应后离子浓度降至1*10-5以下的反应为完全反应。如酸碱中和时[H+]降至10-7mol/L<10-5mol/L,故为完全反应,用“=”,常见的难溶物在水中的离子浓度均远低于10-5mol/L,故均用“=”。
(3)难溶并非不溶,任何难溶物在水中均存在溶解平衡。
(4)掌握三种微溶物质:CaSO4、Ca(OH)2、Ag2SO4
(5)溶解平衡常为吸热,但Ca(OH)2为放热,升温其溶解度减少。
(6)溶解平衡存在的前提是:必须存在沉淀,否则不存在平衡。
2、溶解平衡方程式的书写
3、沉淀生成的三种主要方式
(1)加沉淀剂法:Ksp越小(即沉淀越难溶),沉淀越完全;沉淀剂过量能使沉淀更完全。
(2)调pH值除某些易水解的金属阳离子:如加MgO除去MgCl2溶液中FeCl3。
(3)氧化还原沉淀法:
(4)同离子效应法
4、沉淀的溶解:
沉淀的溶解就是使溶解平衡正向移动。
常采用的方法有:①酸碱;②氧化还原;③沉淀转化。
5、沉淀的转化:
溶解度大的生成溶解度小的,溶解度小的生成溶解度更小的。
如:AgNO3 →AgCl(白色沉淀)→ AgBr(淡黄色)→AgI (黄色)→ Ag2S(黑色)
6、溶度积(Ksp)
1)定义:在一定条件下,难溶电解质电解质溶解成离子的速率等于离子重新结合成沉淀的速率,溶液中各离子的浓度保持不变的状态。
2)表达式:AmBn(s)  mAn+(aq)+nBm-(aq)
mAn+(aq)+nBm-(aq)
Ksp= [c(An+)]m •[c(Bm-)]n
3)影响因素:
外因:①浓度:加水,平衡向溶解方向移动。
②温度:升温,多数平衡向溶解方向移动。
4)溶度积规则
QC(离子积)>KSP 有沉淀析出
QC=KSP 平衡状态
QC<kSP 饱和,继续溶解
第四章 电化学
考点1:原电池的工作原理及应用
1、概念和反应本质
原电池是把化学能转化为电能的装置,其反应本质是氧化还原反应。
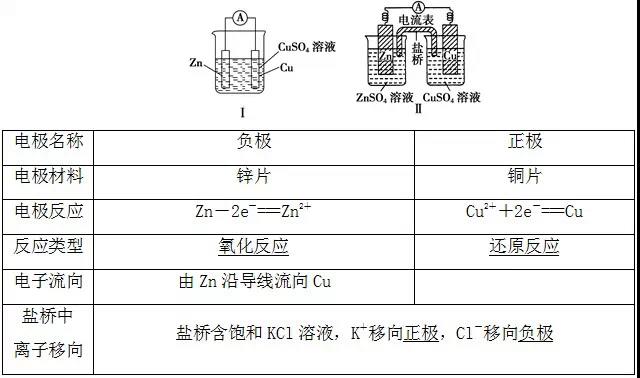
2、工作原理
以铜锌原电池为例
考点2:电解的原理
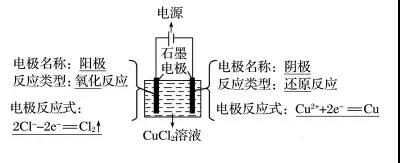
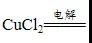
(2)电子和离子的移动方向
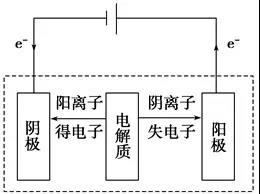
①电子:从电源负极流出后,流向电解池阴极;从电解池的阳极流出后流向电源的正极。
②离子:阳离子移向电解池的阴极,阴离子移向电解池的阳极。

(2)阳极:若是活性电极(金属活动顺序表Ag以前的金属)作阳极,则活性电极首先失电子,电极溶解,溶液中的阴离子不能失电子。
若是惰性电极(Pt、Au、石墨)作阳极,则再看溶液中的阴离子的失电子能力。放电顺序为

5、电解不同溶液的情况对比
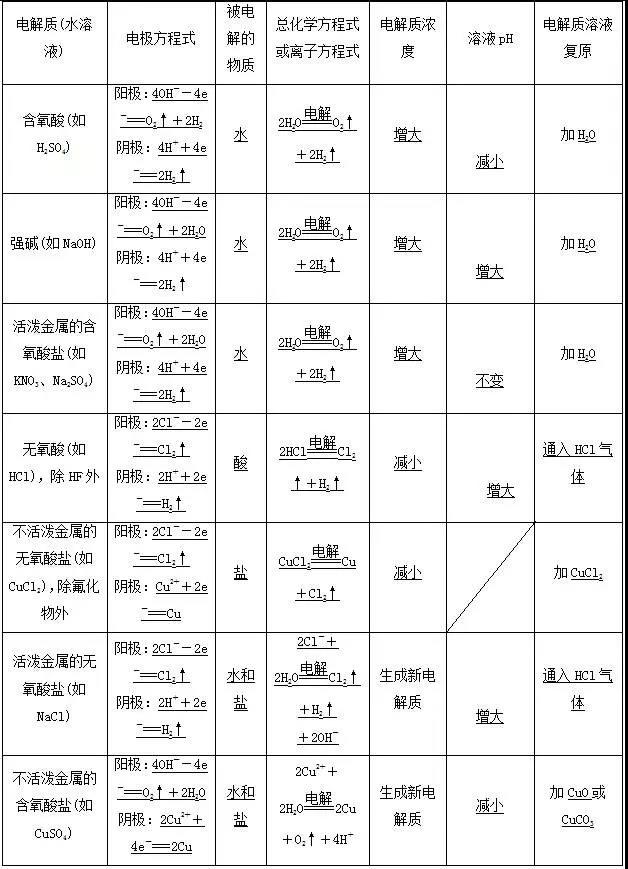
考点3:化学电源
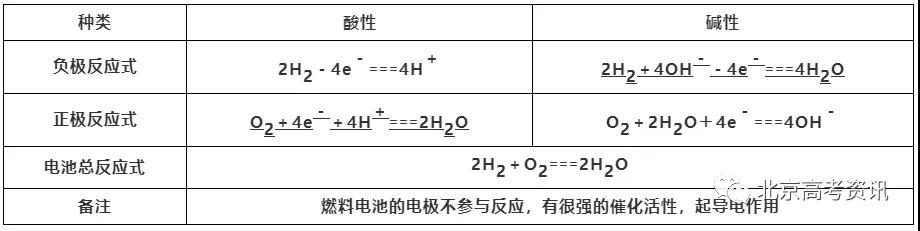
考点4:电解原理的应用
 2NaOH+H2↑+Cl2↑
2NaOH+H2↑+Cl2↑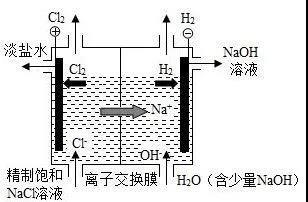
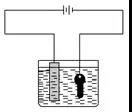
②电解质溶液是AgNO3溶液等含镀层金属阳离子的盐溶液。
③电极反应:
 2Na+Cl2↑
2Na+Cl2↑ 4Al+3O2↑
4Al+3O2↑考点5:金属的腐蚀和保护
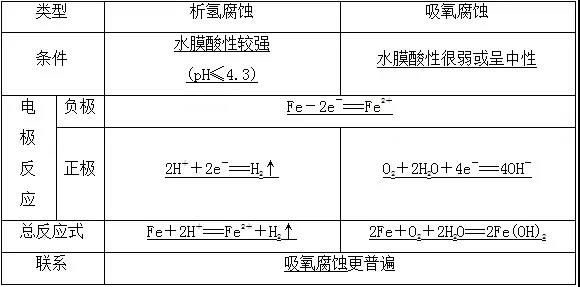
1、金属腐蚀的本质
金属原子失去电子变为金属阳离子,金属发生氧化反应。
2、金属腐蚀的类型
(1)化学腐蚀与电化学腐蚀
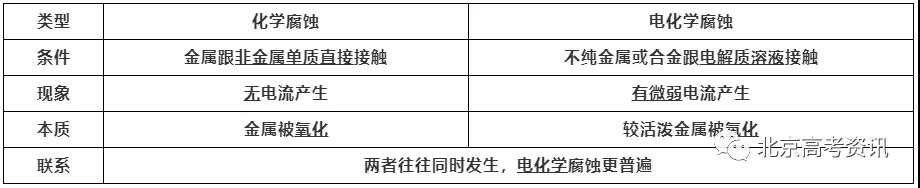
以钢铁的腐蚀为例进行分析: